Natriumnitrid
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
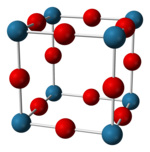
| |||||||||||||
| _ N3− _ Na+ | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Natriumnitrid | ||||||||||||
| Andere Namen |
Trinatriumnitrid | ||||||||||||
| Verhältnisformel | Na3N | ||||||||||||
| Kurzbeschreibung |
dunkelblauer Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 82,98 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest | ||||||||||||
| Dichte |
1,84 g·cm−3[2] | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Natriumnitrid ist eine instabile anorganische chemische Verbindung des Natriums aus der Gruppe der Nitride.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Natriumnitrid kann durch thermische Zersetzung von Natriumazid oder Reaktion von Natriumazid mit Natrium gewonnen werden.[4]
Ebenfalls möglich ist die Herstellung durch Reaktion von Natrium mit Stickstoff in einer elektrischen Entladung.[1]
Eine neuere Synthese beschreibt die Darstellung in einer Vakuumkammer, in der atomares Natrium mit Stickstoff auf ein gekühltes Saphirsubstrat aufgebracht und anschließend auf Raumtemperatur erwärmt wird.[5]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Natriumnitrid ist ein dunkelblauer Feststoff.[1] Er ist extrem instabil und zersetzt sich bei leichter Erwärmung in seine Elemente.[6] Seine Kristallstruktur kann dem anti-Rhenium(VI)-oxid-Typ zugeordnet werden und zeichnet sich durch eine extrem niedrige Raumerfüllung aus.[5]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Ralf Steudel: Chemie der Nichtmetalle: Von Struktur und Bindung zur Anwendung. Walter de Gruyter, 2008, ISBN 3-11-021128-9, S. 310 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Das Periodensystem online: Eigenschaften von Natriumnitrid
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ H. Wattenberg: Über zwei Bildungsweisen von Natriumnitrid und Kaliumnitrid. In: Berichte der deutschen chemischen Gesellschaft (A and B Series). 63, 1930, S. 1667–1672, doi:10.1002/cber.19300630708.
- ↑ a b Rainer Niewa: Na3N – ein origineller Syntheseweg für ein lange gesuchtes binäres Nitrid. In: Angewandte Chemie. 114, 2002, S. 1777–1778, doi:10.1002/1521-3757(20020517)114:10<1777::AID-ANGE1777>3.0.CO;2-Z.
- ↑ Peter Urben: Bretherick's Handbook of Reactive Chemical Hazards: 2-Volume Set. Academic Press, 2006, ISBN 0-08-052340-4, S. 1863 (eingeschränkte Vorschau in der Google-Buchsuche).